2022年5月2日,必赢电子游戏网站杰出校友、国家纳米科学中心聂广军团队在Nature Biomedical Engineering期刊发表论文【1】,通过对大肠杆菌进行基因工程改造,开发了一种基因工程菌来源的基于外膜囊泡(Outer Membrane Vesicles,OMV)的口服肿瘤疫苗。实现口服有效激活肿瘤抗原特异性免疫反应,发挥抗癌作用。
作为个性化肿瘤免疫疗法,肿瘤疫苗通过使用由基因突变产生的肿瘤抗原来激活特定的细胞毒性 T 淋巴细胞(CTL),然后攻击肿瘤细胞。
目前,全世界范围内,已有多款肿瘤疫苗处于临床试验阶段,但这些临床试验中的肿瘤疫苗基本都是通过肌肉注射或皮下注射进行,其中免疫刺激仅限于有限数量的引流淋巴结。由于抗原呈递细胞(APC)在肌肉组织和皮下的分布有限,因此需要佐剂来提高通过这些途径施用的肿瘤疫苗的免疫原性。
实际上,肠道是人体最大的免疫器官,包含了约70%的人体免疫细胞,因此可口服的肿瘤疫苗是引发强烈抗肿瘤免疫反应的有希望的替代选择。此外,与注射相比,口服给药通常被认为具有更好的安全性、更好的患者依从性,以及更低的医疗费用。
然而,由于复杂的胃肠道环境和肠上皮屏障的存在,口服肿瘤疫苗受到了很大限制。理想的口服肿瘤疫苗必须耐受胃肠道环境,才能到达肠道并克服肠上皮屏障与丰富的免疫细胞相互作用。近年来,脂质体、聚合物纳米颗粒等作为疫苗递送载体得到了快速发展,但它们作为口服疫苗载体的有效性扔不理想。因此,迫切需要一种新的口服疫苗技术范式。
聂广军团队通过对大肠杆菌进行基因工程改造,建立了一种基因工程菌来源的基于外膜囊泡(OMV)的口服肿瘤疫苗,可在口服后实现肠道中原位可控产生携带肿瘤抗原的 OMV,OMV 能够携带肿瘤抗原一起有效穿越肠上皮屏障,被固有层中的免疫细胞识别,进而有效激活肿瘤抗原特异性免疫反应,从而显著抑制肿瘤生长、限制肿瘤转移,并发挥长期保护作用。


聂广军研究员(左),赵潇研究员(右)
早在2013年,聂广军团队就在Biomaterials期刊发表了将外泌体作为化疗药物递送平台来治疗癌症的研究论文。谷歌学术显示被引用次数高达1159次,也是国内最早的一批外泌体研究论文之一。
随着研究的深入,外泌体存在一些难以突破的限制,例如产量低,提取难,成分复杂等等。而此时,另外一种天然来源的纳米颗粒——革兰氏阴性细菌来源的OMV,受到了聂广军研究员的关注。
OMV由于携带了丰富的病原体相关分子模式(PAMP),可以激活宿主免疫系统。肠道细菌同样可以分泌OMV,并通过 OMV 与宿主免疫系统相互作用。更重要的是,肠道细菌分泌的 OMV 能够穿过肠上皮屏障并与免疫细胞,尤其是发挥抗原呈递作用的树突状细胞(DC)相互作用,发挥免疫调节能力。
肿瘤疫苗通常需要通过佐剂来提高免疫原性,而 OMV 本身就可以作为天然佐剂,从而实现肿瘤疫苗和佐剂的合而为一。肠道细菌如大肠杆菌很容易进行基因工程改造,也容易发酵和扩大生产规模,从而大量、快速获取 OMV。此外,新西兰、澳大利亚等地应批准了一些 OMV 作为传染病治疗药物,这也证明了其安全性和有效性。
基于 OMV 的种种优势,聂广军团队和赵潇团队于2021年4月在Nature Communications期刊发表论文【2】,提出并开发了一种基于 OMV 的通用肿瘤疫苗平台,将肿瘤抗原与OMV 表面的ClyA 蛋白融合,从而在 OMV 表面展示肿瘤抗原,用以诱导肿瘤抗原特异性抗肿瘤免疫反应。这也为后续的口服肿瘤疫苗的开发奠定了基础。

在上述研究的基础上,聂广军团队对肠道中最丰富的共生菌之一的大肠杆菌,进行基因工程改造,以开发基因工程细菌来源的口服肿瘤疫苗。
首先,将肿瘤抗原(Ag)和小鼠免疫球蛋白 G 的 Fc 片段(mFc)融合 ClyA 蛋白的 C 端,ClyA 蛋白是 OMV 表面最丰富的蛋白之一。mFc 将通过 Fc 和新生儿 Fc 受体(FcRn)之间的相互作用增强树突状细胞(DC)对 OMV 的识别和摄取。
虽然发现大多数基因工程细菌在口服24小时后被清除,但为了安全起见,还需要控制携带肿瘤抗原的 OMV 的产生,以避免长期抗原刺激引起的免疫耐受。研究团队引入了阿拉伯糖(Ara)诱导型启动子来控制融合蛋白的表达。只有在阿拉伯糖存在的情况下,才会诱导融合蛋白的表达,否则表达处于关闭状态。
口服上述基因工程细菌和诱导剂阿拉伯糖后,就能实现在肠道中原位可控地产生携带肿瘤抗原的外膜囊泡——OMV-Ag-mFc。
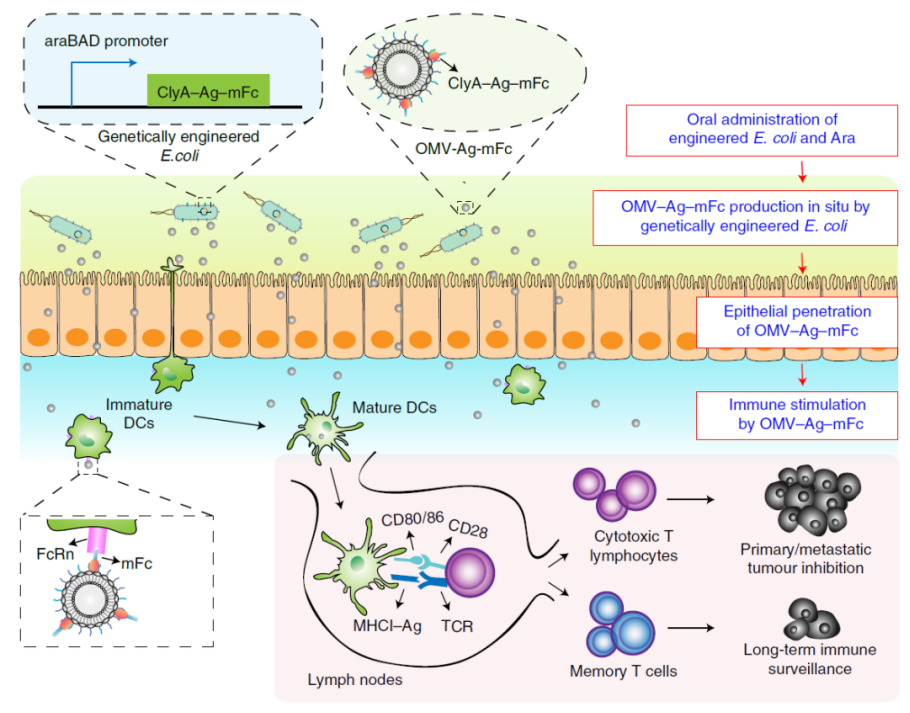
小鼠模型实验显示,这些 OMV-Ag-mFc能够有效地穿过肠上皮屏障并被肠道固有层中的树突状细胞(DC)摄取,然后产生引流淋巴结和肿瘤抗原呈递。肿瘤抗原特异性免疫激活,并在多种小鼠癌症模型中发挥抗肿瘤作用,显著抑制肿瘤生长。
在肺转移性黑色素瘤小鼠模型和皮下结肠肿瘤小鼠模型中,OMV-Ag-mFc能够显著抑制肿瘤生长、减少肿瘤转移,并发挥长期保护作用,防止肿瘤的再次复发和攻击。

总的来说,该研究通过对大肠杆菌进行基因工程改造,建立了一种基因工程菌来源的基于OMV的口服肿瘤疫苗,可在口服后有效激活肿瘤抗原特异性免疫反应,从而显著抑制肿瘤生长、限制肿瘤转移,并发挥长期保护作用。OMV作为肿瘤疫苗载体潜力很大,除了用来展示和递送肿瘤抗原,还可以递送 mRNA,开发 mRNA 肿瘤疫苗。
2022年3月,聂广军团队和赵潇团队在Advanced Materials期刊发表论文【3】,使用OMV作为 mRNA 递送平台,通过基因工程对其进行RNA 结合蛋白L7Ae和溶酶体逃逸蛋白李斯特菌溶血素O的表面修饰——OMV-LL。OMV-LL 可以通过 L7Ae 结合 mRNA 抗原并将它们递送到树突状细胞中,然后通过李斯特菌溶血素O 介导的内体逃逸进行交叉呈递。

这项研究是首次探索 OMV 作为 mRNA 疫苗递送载体,并展示了令人印象深刻的效果,OMV-LL-mRNA 能够显著抑制小鼠黑色素瘤进展,导致37.5%的结直肠癌小鼠模型的肿瘤完全消退。OMV-LL-mRNA 可诱导长期免疫记忆,在60天后仍能保护小鼠免受肿瘤攻击。
而在2021年7月,聂广军团队还在Science Translational Medicine期刊发表了一项引起广泛关注的研究论文【4】。该研究开创性地将大肠杆菌细胞质膜和自体肿瘤细胞膜整合到纳米颗粒中,开发出了新型个性化癌症疫苗,动物实验结果表明,在手术切除肿瘤后,这些杂合膜纳米颗粒诱导了强烈的肿瘤特异性免疫反应,提高了小鼠的存活率,能够长期保护小鼠免受肿瘤的再次攻击。

这项研究表明,基于细菌细胞质膜有效激活先天免疫系统的个性化自体肿瘤抗原疫苗,在癌症术后患者的个性化治疗方面具有巨大潜力。目前已经开始跟北京的几家三甲医院合作,开展研究者发起的临床试验(IIT),患者将涉及非小细胞肺癌到罕见肿瘤。后续还将进一步开发基于这种方法的通用型肿瘤疫苗。
近年来,利用基因工程微生物来递送治疗药物或利用基因工程微生物本身作为作为治疗剂,受到了越来越多的关注。聂广军团队的一系列突破性研究为基于基因工程微生物的治疗应用开辟了更为广阔的前景。
论文链接:
1.https://www.nature.com/articles/s41551-022-00886-2
2.https://www.nature.com/articles/s41467-021-22308-8
3.https://onlinelibrary.wiley.com/doi/abs/10.1002/adma.202109984
4.https://stm.sciencemag.org/content/13/601/eabc2816.full
消息来源:生物世界微信公众号
聂广军研究员简介

聂广军,中科院特聘研究员,国科大特聘教授;科技部纳米研究国家重大科学研究计划(973)项目首席科学家(2012-2016),国家重点研发计划首席科学家(2018-2022);国务院享受政府特殊津贴专家;基金委创新群体、中科院创新交叉团队、中科院卢嘉锡国际团队成员;2016年获中国药学会以岭药业青年科学家奖,美国Houston Methodist Research Institute(休斯敦)兼职教授,英国医学科学院Advanced Newton Scholar;中国生物物理学会常务理事,中国抗癌协会纳米肿瘤学专业委员会委员,中国药学会纳米药物专业委员会委员;国家纳米科学中心科技处处长;Nano Letters 副主编。
1999年于必赢电子游戏网站获得硕士学位,2002年于中国科学院生物物理所获得博士学位,之后在加拿大McGill大学从事博士后研究。2008年回国在国家纳米科学中心建立了“纳米生物学和纳米生物材料”实验室,组建了一个多学科交叉研究团队。课题组现有研究员3名,副研究员3名,助理研究员2名,博新计划博士后2名。课题组已先后获得几十项各类科研资助,主持了多项科技部、基金委、中科院、北京市科委、国际合作项目以及横向合作项目等。与美国、英国、澳大利亚及加拿大等纳米医学和生命科学的多个著名实验室建立了良好的合作关系,先后与6位中科院特聘访问教授开展科研合作。课题组先后培养19名博士、8名博士后、17名硕士。先后获得中国科学院优秀导师奖、中国科学院SABIC-CAS奖学金导师奖、中国科学院澳大利亚必和必拓(BHP Billiton)导师科研奖等教学奖。获得天津市科技进步奖公益类一等奖、中国抗癌协会科技奖一等奖等奖项。
在Nature Biotechnology, Nature Biomedical Engineering, Nature Communications, Blood, JACS, JBC, Angew Chem Int Ed, Adv Mater, Nano Letters, ACS Nano, Adv Funct Mater, Biomaterials, Haematologica, Brit J Haematol, Antioxid Redox Sign, Cancer Letters, Small和Nanomedicine等发表论文140余篇;申请抗肿瘤应用等相关发明专利40余项(授权中国专利20余项,美国授权专利3项,日本专利1项,专利转让2项)。相关研究成果被Nature Biotechnology, Nature Materials, Nature Biomedical Engineering, Nature Reviews of Cancer, Science Translational Medicine和Blood等进行了重点推荐和报道。