近日,必赢电子游戏网站杰出校友、中国科学院分子细胞科学卓越创新中心季红斌研究员在《细胞》杂志的一篇最新资源论文中带来重要突破。研究通过全面的蛋白质基因组学表征,为中国SCLC患者的肿瘤发生、潜在预后生物标志物和免疫景观提供了全新见解,并且为不同亚型的SCLC指出了特异性的潜在治疗策略。同济大学附属上海市肺科医院张鹏教授、中国科学院上海药物研究所周虎研究员、中国科学院分子细胞科学卓越创新中心季红斌研究员与高大明研究员为论文共同通讯作者。

在这项研究中,作者首先从112例接受了手术切除的中国SCLC患者体内,收集了原发性肿瘤及手术切除的癌旁组织作为配对样本,并且对样本进行了涵盖基因组、转录组学、蛋白质组学和磷酸化蛋白质组学的全面蛋白质基因组学表征。
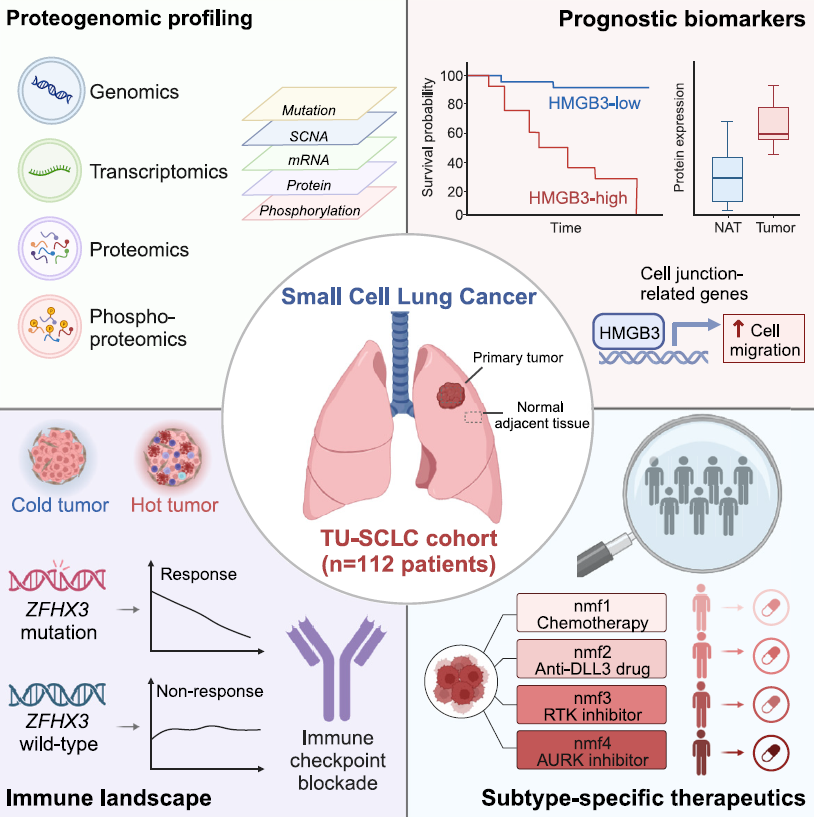
▲最新研究对小细胞肺癌进行了全面的蛋白质基因组学表征,并取得一系列与治疗相关的重要发现(图片来源:参考资料[1])
其中,研究确认了TP53和RB1是SCLC中最常见的突变类型,仅有9位(8%)的患者样本没有出现基因组水平上的TP53或RB1改变,支持了TP53和RB1失活在SCLC肿瘤发生中的关键作用。
一直以来,SCLC的预后非常不理想。在这项研究中,研究团队从分析结果中确认了两个有助于评估疾病复发与进展可能性的潜在预后生物标志物——CASP10和HMGB3。
其中,CASP10是Caspase家族(一类执行细胞凋亡的蛋白)的一员,可以通过影响凋亡、代谢或表观遗传重编程途径抑制肿瘤发生。最新研究发现,SCLC中CASP10的表达水平较低,且与患者预后较差相关。当然,论文也指出,还需要进一步的研究以确认CASP10分子对SCLC肿瘤发生的贡献。
最新研究揭示的另一个潜在预后生物标志物是HMGB3。此前的研究已经发现,HMGB3在各种癌症类型中高度表达,可以驱动癌症转移和生长;而HMGB3表达下调可以抑制多种癌细胞的迁移和侵袭,但其中的机制尚未被揭示。而最新研究发现,HMGB3的过表达通过调节细胞连接相关基因的转录,起到促进SCLC细胞迁移的效果。
值得一提的是,研究数据还表明,HMGB3通过转录依赖的方式与PI3K-Akt和MAPK信号通路相关。此前已经有研究在结直肠癌和胶质母细胞瘤中观察到,HMGB3与PI3K-Akt和MAPK信号通路激活相关。因此这些结果提示我们,HMGB3不仅可以作为SCLC患者的预后生物标志物,还可能在促进SCLC肿瘤发生中起着尚未完全理解的重要、复杂作用。
图片来源:123RF
研究还为更加精准的肿瘤免疫治疗提供了重要线索。通过蛋白质基因组学分析,作者对SCLC的免疫景观进行了表征,从中揭示了ZFHX3突变与高度免疫浸润之间的关联,在临床上证实ZFHX3突变可能作为接受免疫治疗的SCLC患者的潜在预测生物标志物。此外,DNA损伤应答活性的增加还可能通过抑制cGAS-STING通路,起到潜在的免疫抑制作用。
最后,借助机器学习算法对多组学数据进行聚集分类,107份SCLC肿瘤样本被划分为4个不同的亚型(nmf1~nmf4)。这些亚型各自表现出特异性的治疗脆弱性:例如,nmf2亚型高度表达DLL3,提示可能对双特异性抗体疗法Tarlatamab等抗DLL3药物有更好的应答;而nmf3亚型具有RTK信号上升的特征,因此更可能从安罗替尼等RTK抑制剂的治疗中获益。这些亚型与相应特征的发现,将有助于指导SCLC的临床治疗选择。
这项最新工作不仅是中国团队2024年在生物医学领域的CNS开篇之作,也是探索SCLC疗法的重要起点。我们期待,这些重要发现不仅为基础与临床研究提供有价值的资源,也将为我们带来更加有效的SCLC创新疗法,让这种致命癌症有药可治。
参考资料:
[1] Liu et al. Proteogenomic characterization of small cell lung cancer identifies biological insights and subtype-specific therapeutic strategies. Cell (2024). https://doi.org/10.1016/j.cell.2023.12.004
消息来源:学术经纬微信公众号
季红斌研究员简介

1991-1995年就读于bwin必赢登录入口官网获学士学位,1995-2000年就读于中国科学院上海生化与细胞所获博士学位,2000-2007年在哈佛医学院从事博士后工作。2007年受聘于中科院上海生科院生化与细胞所,任研究员、博导。长期从事肺癌发病分子机理的研究,取得一系列原创性的科研成果。迄今为止发表论文130余篇,其中作为第一或通讯作者在Nature, Cancer Cell, Nature Genetics, Journal of Clinical Investigations, Journal of Clinical Oncology, PNAS 等期刊发表论文60余篇。荣获奖励包括上海市“浦江人才计划”, 中科院上海分院系统杰出青年科技创新人才, 国家杰出青年基金, 第七届上海青年科技英才, 上海市优秀学术带头人, 上海医学科技奖二等奖,上海市科技进步二等奖等。现任《中华肿瘤杂志》、Thoracic Cancer、《中国肺癌杂志》等期刊编委;中国抗癌协会上海市分子靶向治疗及免疫治疗委员会副主委,中国抗癌协会肿瘤转移专业委员会、中国抗癌协会肺癌专业委员会、中国医疗保健国际交流促进会胸部肿瘤分会委员。